压力促癌转移实锤!即便压力退场,体内的“促癌记忆”却已生效
当我们谈论慢性压力对健康的危害时,可能自然而然会想到癌症的发生和转移。以往,科学家们多关注压力瞬间飙升的激素,它们如同身体的“警报器”,能直接改变肿瘤微环境,为癌细胞扩散创造条件。
但有时候,压力源明明已经消失,患者体内的应激激素水平也已恢复正常,为何癌症转移的风险却依然居高不下?难道压力在身体里埋下了某种“定时炸弹”?
近期,来自中山大学附属第六医院的研究团队发表于Gut的一项研究可以说另辟蹊径,从人体的“第二大脑”肠道微生物的角度,揭示了慢性压力会持久地扰乱肠道菌群的平衡,而这种失衡及其产生的特定代谢物,竟能在压力激素退潮后,继续为癌细胞的远程扩散“煽风点火”。

DOI:10.1136/gutjnl-2025-335627
一、研究背景与目的
肿瘤转移是癌症患者最主要的死亡原因。慢性心理压力通过激活神经内分泌系统,释放皮质酮等应激激素,已被证明能直接促进肿瘤血管生成、抑制免疫监视,从而助推转移。然而,这只解释了压力期间的即时效应。
近年来,肠道菌群作为全身健康的“调控器”备受关注。其紊乱与多种癌症的发生、发展及治疗反应密切相关。菌群通过产生大量代谢物进入血液循环,远程影响远端器官。
那么,压力是否会破坏菌群平衡,而失调的菌群及其代谢产物,在压力过后又会不会持续“作祟”,驱动转移?
二、研究方法及结果
研究人员首先在小鼠中建立慢性束缚应激模型。他们在压力停止、小鼠血液中的应激激素(皮质酮)水平完全恢复正常后,才进行多种癌症(如结肠癌、乳腺癌)的转移模型接种。
结果显示:经历过慢性压力的小鼠,其肺或肝部的转移瘤负荷显著高于从未经历压力的对照组。
也就是说,压力的促转移效应具有“记忆”,能在压力源消失后持续存在。
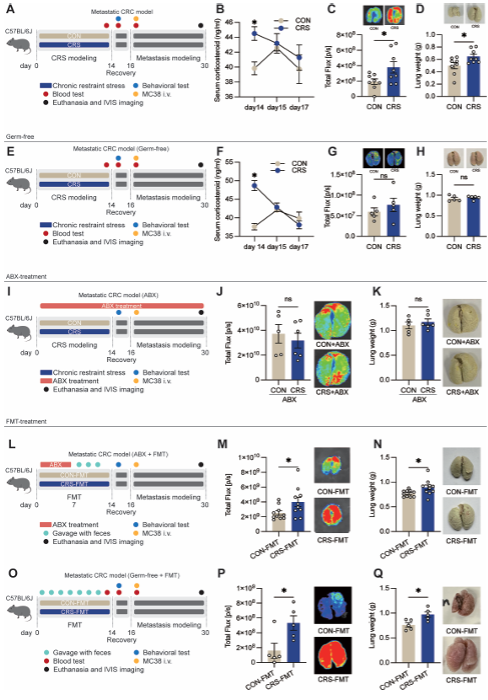
微生物群是慢性压力促进癌症转移的必要条件
排除了激素的直接作用后,研究者利用先进的鸟枪法宏基因组测序和代谢组学技术,分析了压力后小鼠的肠道菌群和血液代谢物。他们发现了两个关键变化:
菌群层面:有益菌,动物双歧杆菌的丰度急剧下降。
代谢物层面:血液和粪便中一种名为油酸的单不饱和脂肪酸水平异常升高。
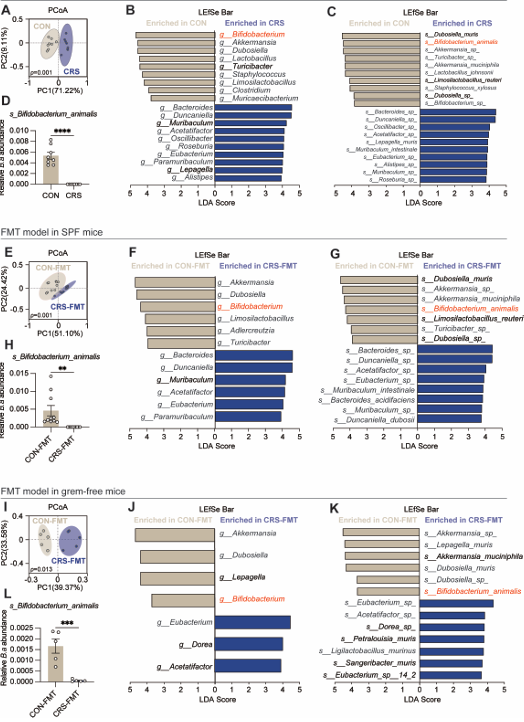
长期压力会对微生物群产生影响,导致动物双歧杆菌数量减少
接下来,研究人员进行了因果验证,他们首先给经历压力后的小鼠补充动物双歧杆菌。结果,小鼠体内油酸水平显著降低,肿瘤转移被有效抑制。反之,给正常小鼠直接补充油酸,竟能模拟出慢性压力的效果,显著增加转移灶。
体外实验进一步表明油酸能直接增强癌细胞的迁移和侵袭能力。
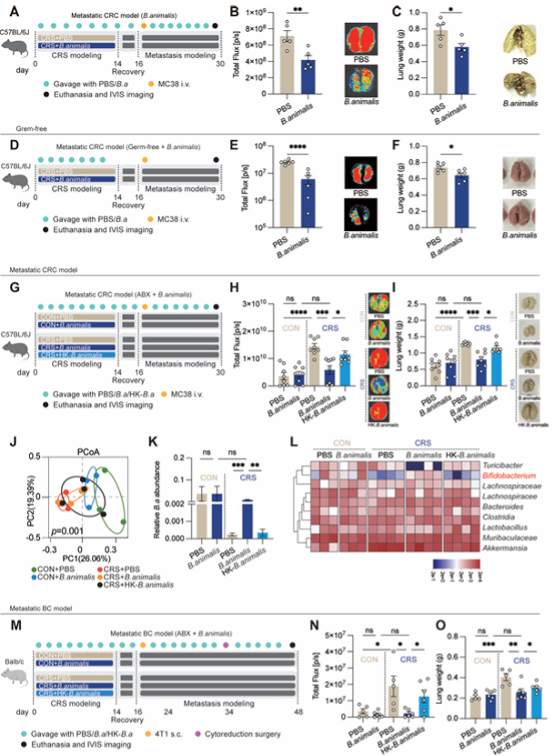
动物双歧杆菌抑制应激相关转移
那么经历压力究竟为何会减少动物双歧杆菌丰度?该菌又如何影响油酸?
研究人员通过基因组分析发现,动物双歧杆菌携带一个名为“油酸水合酶”的特殊基因,该酶能有效降解油酸。因此,这种菌丰度减少,油酸自然堆积。
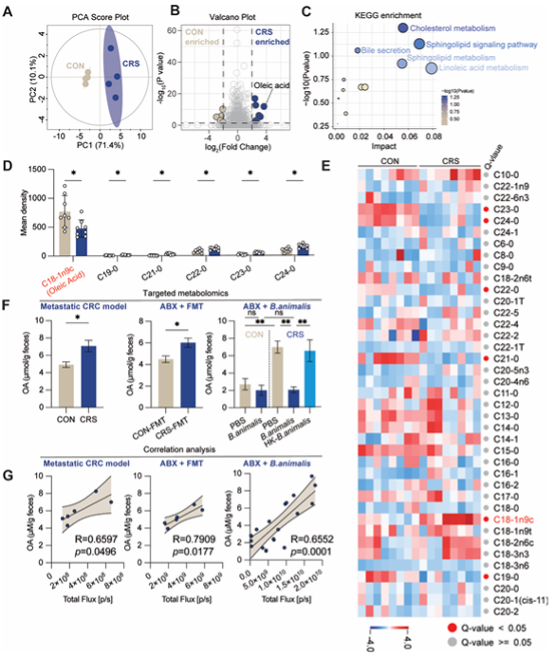
慢性压力导致肠道管腔内油酸富集
进一步研究发现,压力下的高浓度皮质酮并非直接杀菌,而是通过改变肠道上皮细胞的嘌呤代谢,导致鸟嘌呤这种核苷消耗增加。而鸟嘌呤正是动物双歧杆菌生长必需的“营养”。压力激素通过“饿死”有益菌的间接方式,导致了菌群失调。
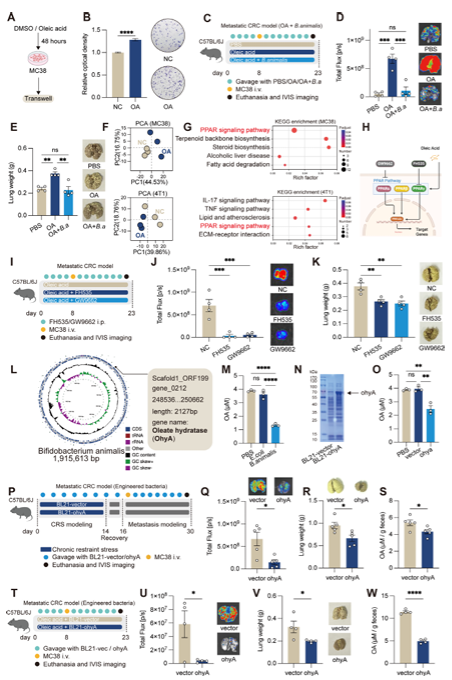
动物双歧杆菌及BL21-ohyA工程菌可抵消压力诱导的肿瘤转移
在结直肠癌患者队列中,研究者又发现了高度一致的证据:高压力评分的患者,粪便中动物双歧杆菌丰度和油酸水合酶基因表达更少,血液和粪便中油酸水平更高,且发生癌症转移的比例显著增加。这强力证实了该机制在人类疾病中的相关性。
三、总结
这项研究首次将心理压力、肠道上皮代谢、关键益生菌的存亡、特定代谢物的累积以及最终的癌症转移串联成一条完整的逻辑链条。
这项发现具有重要的转化医学意义。它提示我们,管理压力、维护肠道健康可能是抗癌的重要一环。未来,通过补充特定的益生菌(如动物双歧杆菌)、开发靶向油酸降解酶的微生态制剂、或监测血液油酸水平作为风险预警标志,都可能成为预防癌症转移、改善患者预生的有效新策略。



